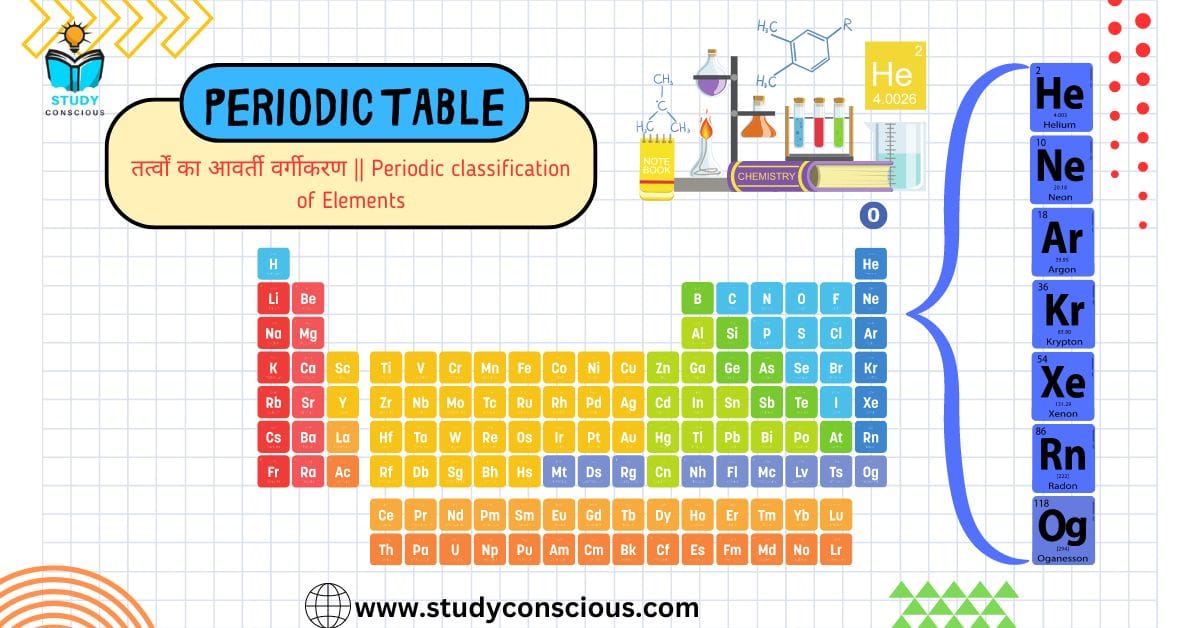
तत्वों का आवर्ती वर्गीकरण (Periodic Classification of Elements) एक वैज्ञानिक प्रणाली है जिसमें तत्वों को उनकी भौतिक और रासायनिक गुणों के आधार पर वर्गीकृत किया गया है। यह वर्गीकरण आवर्त सारणी (Periodic Table) के रूप में प्रस्तुत किया गया है। आवर्त सारणी में तत्वों को उनके परमाणु क्रमांक के अनुसार क्रमबद्ध किया गया है, और यह सारणी उनके आवर्ती गुणों को दर्शाती है।

मुख्य बिंदु:
- आवर्त सारणी का निर्माण:
- पहली आवर्त सारणी का निर्माण दिमित्री मेन्डलीव ने 1869 में किया था। उन्होंने तत्वों को उनके परमाणु भार के आधार पर क्रमबद्ध किया और उनके गुणधर्मों के आवर्ती पैटर्न का अध्ययन किया।
- आधुनिक आवर्त सारणी में तत्वों को उनके परमाणु क्रमांक (Atomic Number) के आधार पर क्रमबद्ध किया जाता है।
- आवर्त नियम (Periodic Law):
- आवर्त नियम कहता है कि तत्वों के भौतिक और रासायनिक गुणधर्म उनके परमाणु क्रमांक के आवर्ती फलन होते हैं।
- आवर्त सारणी के प्रमुख समूह:
- क्षार धातुएँ (Alkali Metals): समूह 1 (H को छोड़कर) – जैसे लिथियम (Li), सोडियम (Na), पोटैशियम (K)।
- क्षार मृदा धातुएँ (Alkaline Earth Metals): समूह 2 – जैसे मैग्नीशियम (Mg), कैल्शियम (Ca)।
- हैलोजन (Halogens): समूह 17 – जैसे फ्लोरीन (F), क्लोरीन (Cl)।
- नोबल गैसें (Noble Gases): समूह 18 – जैसे हीलियम (He), निऑन (Ne), आर्गन (Ar)।
- आवर्त सारणी के प्रमुख आवर्त (Periods):
- आवर्त सारणी में कुल 7 आवर्त (Horizons) होते हैं, जिनमें तत्व उनके परमाणु क्रमांक के अनुसार व्यवस्थित होते हैं।
- आवर्त सारणी का महत्व:
- यह तत्वों के गुणधर्मों का पूर्वानुमान लगाने में सहायक होती है।
- विभिन्न रासायनिक प्रतिक्रियाओं और यौगिकों के निर्माण को समझने में मदद करती है।
- रासायनिक अनुसंधान और शिक्षा में एक महत्वपूर्ण उपकरण है।
तत्वों के आवर्ती वर्गीकरण से संबंधित कुछ महत्वपूर्ण बिंदु:
- कुल ज्ञात तत्व – 118
- प्रकृति में प्राप्त तत्व – 94
- कृत्रिम विधि से निर्मित तत्व- 24
- धातु तत्वों की संख्या – 91
- अधातु तत्वों की संख्या- 20
- उपधातु तत्वो की संख्या- 7
- भूपर्पटी में सबसे अधिक मात्रा में पाया जाने वाला तत्व – ऑक्सीजन
- भूपर्पटी में सबसे अधिक मात्रा में पाया जाने वाला धातु तत्व – एल्युमिनियम
- सबसे हल्का तत्व – हाइड्रोजन
- सबसे भारी तत्व – ऑस्मियम
- सबसे हल्की धातु तत्व – लीथियम
- द्रव धातु तत्व – पारा
- द्रव अधातु तत्व – ब्रोमीन
- विद्युत की सबसे अच्छी सुचालक धातु तत्व – चॉदी
- विद्युत की सुचालक अधातु तत्व – ग्रेफाइट
- सबसे अधिक आघातवर्द्वनीय तत्व – सोना
- सबसे अधिक क्रियाशील अधातु तत्व – फलोरीन
- सबसे अधिक क्रियाशील धातु तत्व – फांसियम, पोटैशियम
- सर्वाधिक आयनन विभव वाला तत्व – हीलियम
- न्युनतम आयनन विभव वाला तत्व- सीजियम
- सार्वाधिक इलेक्ट्रॉनिक प्राप्ति वाला तत्व – क्लोरिन
- सार्वाधिक विद्युत ऋणात्मक तत्व – फलोरिन
- सबसे प्रबल ऑक्सीकारक पदार्थ – फलोरिन
- मानव शरीर में सर्वाधिक मात्रा मे पाया जाने वाला तत्व – ऑक्सीजन
- मिट्टी के तेल में रखा जाने वाला तत्व- सोडियम
- हड्डियों एवं दाँतो का निर्माण करने वाला तत्व – कैल्शियम
- उत्कृट गैसों को आवर्त सारणी के वर्ग 18 में रखा गया है।
- हैलोजन परिवार की इलेक्ट्राँन बन्धुता घटते का क्रम -f>cl>Br>I है।
- आवर्त सारणी के शून्य वर्ग में सर्वाधिक गैंसीय तत्व (सभी गैसे अक्रिय गैसें व एक परमाण्विक तत्व) है
- जब किसी परमाणु के बाहृातम कोश में एक इलेक्ट्रॉन जोंडा जाता है, तो मुक्त ऊजा इलेक्ट्रॉन बंधुता कहलाती है।
- सर्वाधिक घनत्व वाला तत्व ऑस्मियम है।
- आवर्त सारसी में हाइड्रोजन का कोई निश्चित स्थान न होने के कारण हाइड्रोजन का क्षार धातुओं व हैलोजनों दोनों से समानता रखता है।
- तत्वों का एक्टिनाइड समूह रेडियों सक्रिय समूह कहलाता है।
- अधिकतम कृत्रिम तत्व ऐक्टिनॉइड समूह में रखें गये है।
- च ब्लाक में धातु अधातु व उपधातु सभी प्रकार के तत्व पाये जाते है।
- आंतरिक संक्रमण तत्व लैन्थेनाइट व ऐक्टिनाइड श्रेणी के तत्व कहलाता है।
- आधुनिक आवर्त सारणी में तत्वों को बढ़ते हुए परमाणु क्रमांक में व्यवस्थित किया गया है।
- आवर्त सारणी के ऊर्ध्वाधर स्तम्भों को वर्ग कहते है।
- किसी उदासीन परमाणु से एक इलेक्ट्रॅान निकालने के लिए आवष्यक ऊर्जा की मात्रा को आयनन विभव कहते है।
- मेण्डलीफ के अनुसार तत्वों के गुण आवर्ती फलन परमाणु भार के होते है।
- तत्वों के वर्गीकरण से सम्बंधित त्रिक् के नियम का प्रतिपादन डोबेराइनर किया था।